环泊酚注射液和注射用甲苯磺酸瑞马唑仑有新适应症报产
none="shifuMouseDown('shifu_t_016')" style="margin-top: 5px;padding: 10px;white-space: normal;border-top: none rgb(28, 118, 129);border-right: none rgb(28, 118, 129);border-bottom: none rgb(28, 118, 129);line-height: 25px;color: rgb(153, 153, 153);background-color: rgb(243, 243, 243);box-shadow: rgb(153, 153, 153) 1px 1px 2px;border-left: 10px solid rgb(28, 118, 129);"> CDE总体承办情况
据统计,2021年2月CDE共承办药品注册申请702件。
2020年10月-2021年2月CDE承办药品注册申请情况(按受理号计)

none="shifuMouseDown('shifu_t_016')" style="margin-top: 5px;padding: 10px;white-space: normal;border-top: none rgb(28, 118, 129);border-right: none rgb(28, 118, 129);border-bottom: none rgb(28, 118, 129);line-height: 25px;color: rgb(153, 153, 153);background-color: rgb(243, 243, 243);box-shadow: rgb(153, 153, 153) 1px 1px 2px;border-left: 10px solid rgb(28, 118, 129);"> 一致性评价补充申请承办情况
2021年2月,35个品种的一致性评价补充申请获CDE承办。非洛地平缓释片、缬沙坦分散片、烟酸片、盐酸乐卡地平片、注射用丁二磺酸腺苷蛋氨酸、注射用头孢哌酮钠等6个品种为首次提交一致性评价补充申请。详细情况见下表:
2月CDE补充申请(一致性评价)品种承办情况


none="shifuMouseDown('shifu_t_016')" style="margin-top: 5px;padding: 10px;white-space: normal;border-top: none rgb(28, 118, 129);border-right: none rgb(28, 118, 129);border-bottom: none rgb(28, 118, 129);line-height: 25px;color: rgb(153, 153, 153);background-color: rgb(243, 243, 243);box-shadow: rgb(153, 153, 153) 1px 1px 2px;border-left: 10px solid rgb(28, 118, 129);"> 新药申请承办情况
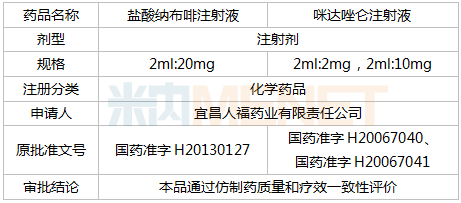
2021年2月,78个品种的新药申请获CDE承办。其中1类新药有55个,2类改良型新药有18个,此外,还有3个3.3类生物类似药。辽宁海思科制药的环泊酚注射液和江苏恒瑞医药的注射用甲苯磺酸瑞马唑仑均有新适应症上市申请。
2月国内新药上市申请承办情况

2月国内新药临床申请承办情况






none="shifuMouseDown('shifu_t_016')" style="margin-top: 5px;padding: 10px;white-space: normal;border-top: none rgb(28, 118, 129);border-right: none rgb(28, 118, 129);border-bottom: none rgb(28, 118, 129);line-height: 25px;color: rgb(153, 153, 153);background-color: rgb(243, 243, 243);box-shadow: rgb(153, 153, 153) 1px 1px 2px;border-left: 10px solid rgb(28, 118, 129);"> 仿制申请承办情况
2021年2月,83个品种的仿制申请获CDE承办,其中38个品种目前已有企业通过或视同通过一致性评价。艾地骨化醇软胶囊、丙酸氟替卡松吸入粉雾剂、布立西坦注射液、碘普罗胺注射液、塞瑞替尼胶囊、色甘酸钠颗粒、右酮洛芬氨丁三醇注射液等7个品种为首仿品种。详细情况见下表:
2月国内仿制申请承办情况






none="shifuMouseDown('shifu_t_016')" style="margin-top: 5px;padding: 10px;white-space: normal;border-top: none rgb(28, 118, 129);border-right: none rgb(28, 118, 129);border-bottom: none rgb(28, 118, 129);line-height: 25px;color: rgb(153, 153, 153);background-color: rgb(243, 243, 243);box-shadow: rgb(153, 153, 153) 1px 1px 2px;border-left: 10px solid rgb(28, 118, 129);"> 进口申请承办情况
2021年2月,51个品种的进口申请获CDE承办。其中1类新药有19个,2类改良型新药有7个,5.1类进口原研药有4个,5.2类进口仿制药有12个。拜耳提交1类新药Finerenone薄膜衣片上市申请,辉瑞提交1类新药阿布昔替尼片上市申请。详细情况见下表:
2月进口上市申请承办情况


2月进口临床申请承办情况


none="shifuMouseDown('shifu_t_016')" style="margin-top: 5px;padding: 10px;white-space: normal;border-top: none rgb(28, 118, 129);border-right: none rgb(28, 118, 129);border-bottom: none rgb(28, 118, 129);line-height: 25px;color: rgb(153, 153, 153);background-color: rgb(243, 243, 243);box-shadow: rgb(153, 153, 153) 1px 1px 2px;border-left: 10px solid rgb(28, 118, 129);"> 获批情况
据米内网MED2.0中国药品审评数据库统计,2021年2月有3个1类新药获批,其中上海君实生物的特瑞普利单抗注射液以及信达生物的信迪利单抗注射液为新适应症获批。此外,正大天晴的盐酸安罗替尼胶囊和阿斯利康的达格列净片均有新适应症获批。
仿制方面,有52个仿制药获批,其中南京海纳医药科技的奥美拉唑碳酸氢钠干混悬剂(Ⅰ)、奥美拉唑碳酸氢钠干混悬剂(Ⅱ)和湖北远大天天明制药的贝美前列素滴眼液为首仿获批。
此外,还有33个品种通过一致性评价(补充申请)。详细情况见下表:
2月上市申请品种及一致性评价品种审批情况






数据来源:米内网MED2.0药品审评数据库、CDE、NMPA;相关统计字段按药品名称统计;药物作用靶点以及适应症来自公开资料。


























 客服微v信:
客服微v信:








 京公网安备 11010802031568号
京公网安备 11010802031568号

